FARMAKOKINETYKA KOENZYMU Q10
Rozdział 2 z publikacji Farmakologia kliniczna koenzymu Q10 , prof. dr hab. med. Józef Drzewoski.
Kinetykę CoQ10 badano m.in. na szczurach wykorzystując preparat znakowany izotopem węgla (C14 CoQ10).[143]. Zwierzęta, przed rozpoczęciem eksperymentu były karmione pokarmem pozbawionym ubichinonu przez dwa tygodnie. Rozmieszczenie C14CoQ10 w różnych tkankach i narządach oceniano po 2, 4, 6, 24, 72 h oraz po 14 dniach od doustnego podania związku. Maksymalną radioaktywność osocza stwierdzono po 2 h. W kolejnych punktach czasowych intensywność promieniowania stopniowo zmniejszała się, aż do całkowitego zaniku po upływie 14 dni. Zwrócono uwagę, że C14CoQ10 gromadził się w największym stopniu w wątrobie, a następnie w nadnerczach, śledzionie, płucach i w sercu. Śladowe ilości wykryto w mózgu, mięśniach, jądrach, grasicy, dziąsłach i w erytrocytach.
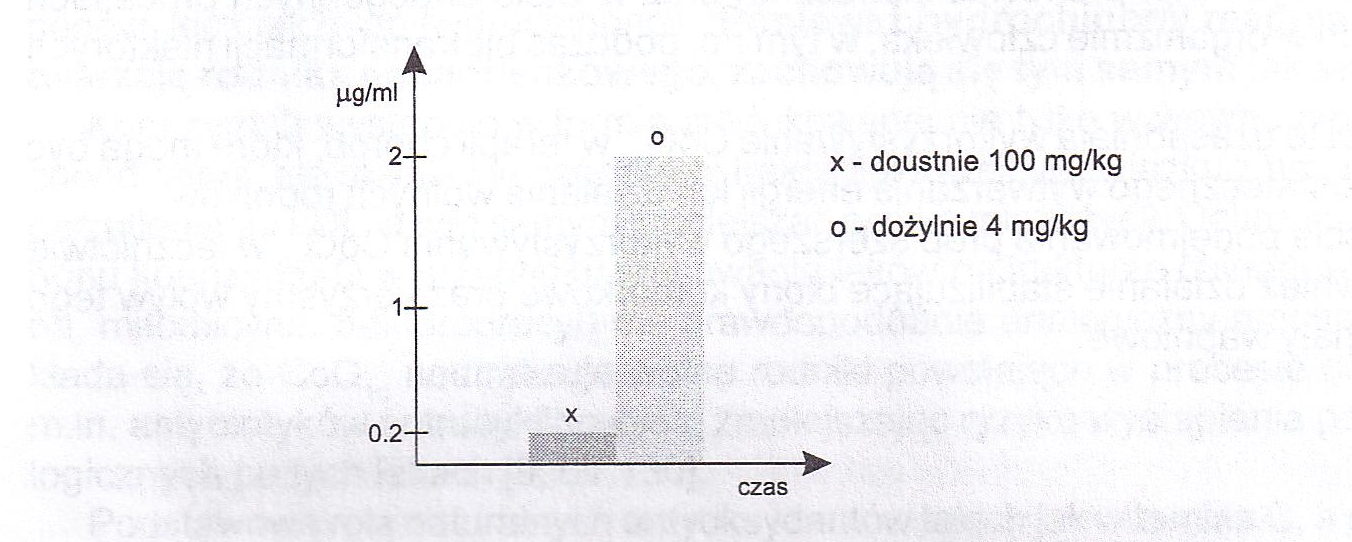
Rycina 3. Stężenie koenzymu Q10 we krwi szczurów po podaniu doustnym i dożylnym wg Scaloriego
Yuzuriha i wsp. [274] badając kinetykę egzogennego CoQ10 u świnki morskiej potwierdzili, że głównym miejscem magazynowania egzogennego CoQ10 jest wątroba. Zaobserwowali ponadto, że pewna ilość związku zgromadzonego w wątrobie jest z niej stopniowo uwalniana do krwiobiegu i przenoszona do innych tkanek i narządów. Dynamika tego procesu zależy od stężenia koenzymu (endogennego + egzogennego) we krwi.
Scalori i wsp.[229] oceniali stężenie CoQ10 w osoczu i w różnych narządach szczura po podaniu związku drogą dożylną, doustną i przezskórną. Wyniki tych badań wykazały również, że ubichinon niezależnie od sposobu podania, gromadzi się przede wszystkim w wątrobie. Duże nagromadzenie CoQ10 w tym narządzie oraz udział w mikrosomalnym systemie utleniania ksenobiotyków, tłumaczy częściowo jego hepatoprotekcyjne działanie u zwierząt doświadczalnych poddanych ekspozycji na czterochlorek węgla.
Po dożylnym wstrzyknięciu CoQ10 w dawce 4mg/kg osiągnięte stężenie w mięśniu sercowym było zbliżone do wartości uzyskanych po doustnym podaniu dawki 25 krotnie większej (100 mg/kg). Wskazuje to na małą biodostępność doustnych postaci CoQ10. Wyniki badań Scaloriego i wsp. [229] sugerują, że w ostrych stanach kardiologicznych lek należy podawać dożylnie (ryc.3). Umożliwiłoby to szybkie uzyskanie wysokich stężeń CoQ10 w uszkodzonym sercu. Nie zapewnia tego podawanie doustnych preparatów ubichinonu. Potwierdzają to również obserwacje Sunamoriego i wsp. [240] (ryc.4).
Stwierdzono, że stężenie maksymalne CoQ10 w sercu po doustnym podaniu substancji egzogennej było znacznie niższe niż w wątrobie. Spostrzeżenie to może wyjaśnić częściowo rozbieżne dane dotyczące skuteczności terapeutycznej ubichinonu u ludzi, zwłaszcza jeśli uwzględni się stosowanie różnych dawek w wielu próbach klinicznych.
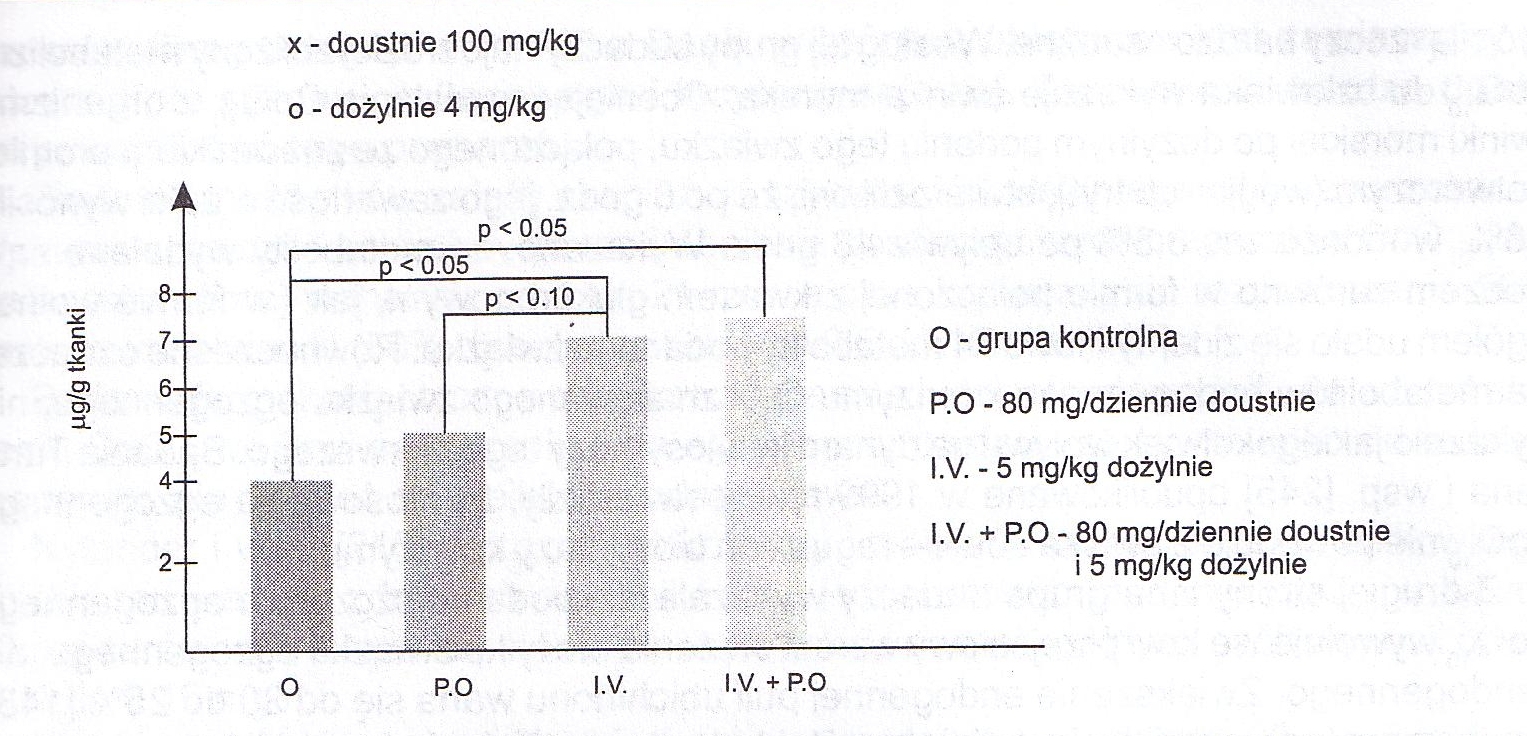
Rycina 4. Średnie stężenie koenzymu Q10 w mięśniu sercowym 44 chorych poddanych zabiegowi pomostowania aortalno-wieńcowego po podaniu dożylnym oraz po łącznym podaniu dożylnym i doustnym jego egzogennej formy wg Sunamori [208]
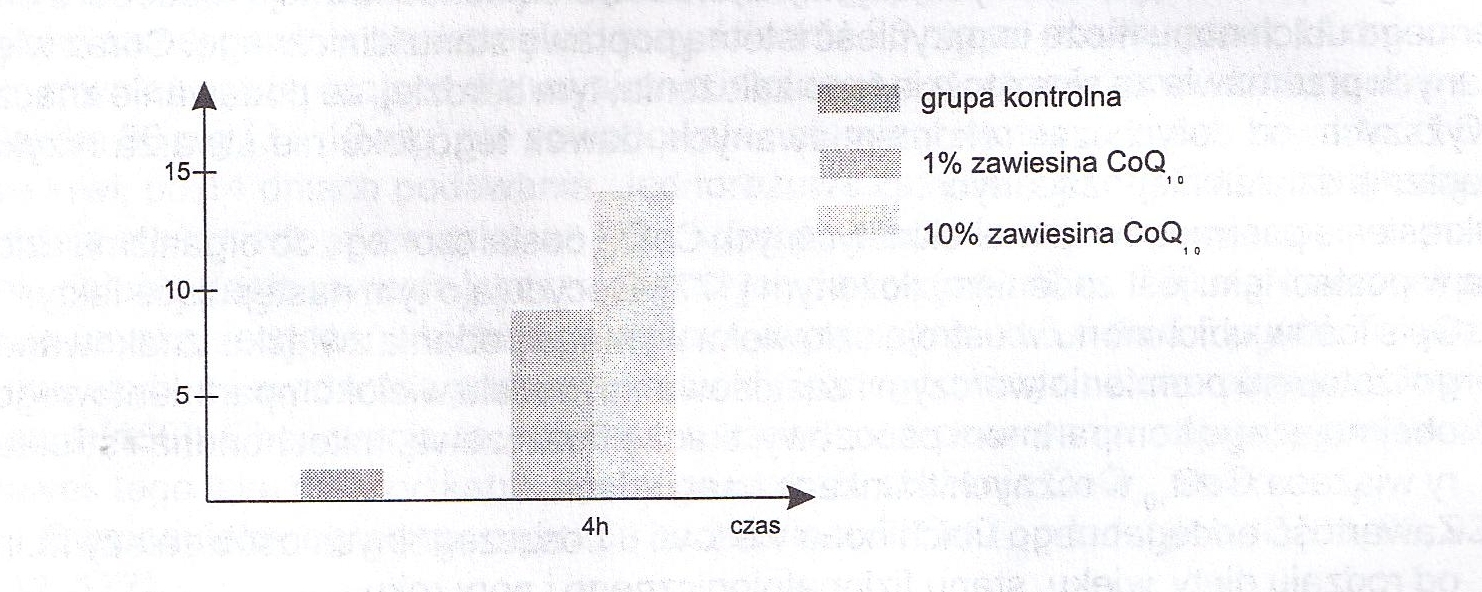
Rycina 5. Stężenie koenzymu Q10 w skórze szczurów w 4 godziny po jego zastosowaniu miejscowym w formie zawiesiny wg Scaloriego [199]
Autorzy ci wykazali również wchłanianie CoQ10 przez skórę i błony śluzowe. Uzasadnia to miejscowe stosowanie CoQ10 w różnych chorobach dermatologicznych i stomatologicznych [105, 120, 171, 261, 272].
Po nałożeniu leku w formie zawiesiny w oliwce na zewnętrzne warstwy skóry, najwyższe stężenie w głębszych warstwach tej tkanki zanotowano po 4 godz. (ryc.5).
Wykazano, że wchłanianie różnych homologów koenzymu Q z przewodu pokarmowego zależy od rodzaju zastosowanego rozpuszczalnika. CoQ10 nie rozpuszcza się w wodzie. Rozpuszcza się natomiast w alkoholu i w tłuszczach roślinnych. W związku z dużą lipofilnością, preparaty ubichinonu zaleca się zażywać bezpośrednio po posiłkach.
Należy jednak podkreślić, na co zwracają uwagę Nakamura i wsp. [203], że koenzym Q10 jest w różnym stopniu przyswajany i metabolizowany przez różne zwierzęta doświadczalne. Dlatego odnoszenie danych uzyskanych w badaniach na zwierzętach do ludzi musi być siłą rzeczy bardzo ostrożne. Według tej grupy badaczy najbardziej zbliżony metabolizm CoQ10 do człowieka wykazuje świnka morska. Oceniając wydalanie CoQ10 z organizmu świnki morskiej po dożylnym podaniu tego związku, połączonego ze znacznikiem promieniotwórczym (węgiel lub tryt), stwierdzili oni, że po 8 godz. jego zawartość w żółci wynosiła 4,6%, w moczu zaś 8,3% po upływie 48 godz. Wykazano, że metabolity wydalane są z moczem zarówno w formie połączonej z kwasem glukuronowym, jak i w formie wolnej. Ogółem udało się zidentyfikować 4 metabolity podanego związku. Równoczesne oznaczanie metabolitów endogennego koenzymu Q10 i znakowanego związku egzogennego, nie wykazało jakiegokolwiek wpływu na dynamikę biosyntezy tego pierwszego. Badania Turunena i wsp. [245] opublikowane w 1999 roku potwierdziły, że stosowanie egzogennego CoQ10 nie powoduje zjawiska down – regulation biosyntezy koenzymu.
Z drugiej strony inna grupa badaczy wykazała, że podanie szczurom egzogennego CoQ10 wywołuje we krwi przejściowy wzrost stężenia nie tylko związku egzogennego, ale i endogennego. Zwiększenie endogennej puli ubichinonu waha się od 20 do 25% [143]. Mechanizm tego zjawiska jest niejasny. Zakłada się możliwość aktywacji biosyntezy lub hamowanie katabolizmu endogennego CoQ10 przez związek egzogenny. Jeśli hipoteza ta jest słuszna, to racjonalnym wydaje się dążenie do uzyskiwania wysokich stężeń ubichinonu we krwi, w tkankach i w narządach poprzez podawanie odpowiednio dużych dawek tego leku. U osób, u których objawy chorobowe są konsekwencją niedoboru endogennego ubichinonu może to przynieść istotną poprawę stanu klinicznego. Coraz więcej danych przemawia za słusznością tego założenia, tym bardziej, że podawanie znacznie wyższych, od dotychczas rekomendowanych, dawek tego leku nie stwarza ryzyka wystąpienia działań niepożądanych.
Określenie parametrów farmakokinetycznych CoQ10 dostarczonego do organizmu człowieka w postaci leku jest zadaniem złożonym [177]. Decydują o tym następujące fakty:
- Opis losów ubichinonu w ustroju człowieka wymaga podania związku znakowanego izotopem promieniotwórczym i zastosowania modelu wielokompartmentowego, obejmującego kompartment osoczowy, tkankę tłuszczową, mitochondria i struktury wiążące CoQ10 w różnych tkankach i narządach.
- Zawartość endogennego ubichinonu we krwi u poszczególnych osób zależy m.in. od rodzaju diety, wieku, stanu fizjopatologicznego i pory roku.
- Doskonała rozpuszczalność CoQ10 w lipidach, sprzyjająca szybkiej dystrybucji jego egzogennej postaci z krwi do innych kompartmentów organizmu.
Kishi i wsp. [143] ocenili biodostępność 6 ze 166 preparatów CoQ10 dostępnych na rynku japońskim. Każdy z tych preparatów (tabletki, granulki, „miękkie” kapsułki) był podawany w dawce 20 mg trzy razy dziennie przez cztery dni, a następnie określano stężenie całkowitego ubichinonu w osoczu. Największe stężenie stwierdzono po zażyciu leku w formie kapsułek. Było ono 2,7 razy wyższe niż po zastosowaniu innych preparatów. W przypadku jednej
z ocenianych tabletek nie stwierdzono żadnych zmian zawartości CoQ10 we krwi. Wyniki tych badań wskazują na istotne znaczenie kliniczne biodostępności różnych form CoQ10 [256]. Stosowanie preparatów o bardzo małej wartości tego parametru sprzyja tzw. „terapii pozornej” i dlatego powinny być one eliminowane z rynku farmaceutycznego.
Pozzi i wsp. [219] wykazali, że kapsułki zawierające ubichinon rozpuszczony w lecytynie sojowej, charakteryzuje największa biodostępność. Pole pod krzywą stężeń leku względem czasu (AUC0-24h ) po podaniu 100 mg CoQ10 w kapsułce było 2-3 krotnie większe niż AUC0-24h obliczone dla trzech porównywanych form tego leku.
Biodostępność leków zależy również od szybkości ich dezintegracji i rozpuszczania. Wykazano, że czas potrzebny do rozdrobnienia poszczególnych preparatów CoQ10 /desintegration time/ wahał się od 1 do 21 min. a czas konieczny do rozpuszczenia 50% zastosowanej dawki /50% dissolution time/ od 0,5 do 10 min [143].
Badania farmakokinetyczne przeprowadzone na ludziach udowodniły, że wzrost stężenia CoQ10 we krwi po podaniu jego egzogennej postaci zależy nie tylko od rodzaju preparatu, ale również od wielkości podanej dawki.
Nylander i wsp.[210] wykazali krótkotrwały i niewielki wzrost stężenia całkowitego ubichinonu we krwi zdrowych ochotników po jednorazowym podaniu CoQ10 w dawce 33 mg zarówno w formie kapsułek, jak i tabletek. U poszczególnych osób wynosił on od 0,01 do 0,19 mg/ml.
Kishi i wsp. [143] stwierdzili po jednorazowym doustnym podaniu 60 mg CoQ10, że czas opóźnienia pojawienia się leku w krwiobiegu po jego zażyciu /lag time/ wahał się pomiędzy 2 a 4 h. Maksymalne stężenie CoQ10 zanotowano po upływie 6 h, przy czym było ono o 37% wyższe niż wyjściowe. Podwyższony poziom CoQ10 utrzymywał się przez 24 h, a następnie stopniowo zmniejszał się, osiągając wartość wyjściową po 96 h. Podanie tej samej dawki wg schematu 3 razy dziennie 20 mg po posiłku przez 14 dni, okazało się również wystarczające dla uzyskania istotnego wzrostu stężenia ubichinonu we krwi. Dawka 30 mg (3 x 10 mg) nie powodowała natomiast istotnych zmian zawartości CoQ10 we krwi, po 14 dniach podawania. Jednorazowe zażycie 120 mg CoQ10 zwiększa dwukrotnie stężenie tego związku we krwi, które powraca do wartości wyjściowych po siedmiu dniach. Zastosowanie jeszcze większych dawek (od 180 do 720 mg/dziennie) powoduje uzyskanie stężeń ubichinonu we krwi w granicach od 3,5 do 5,5 mg / ml. Towarzyszy temu szybka i ewidentna poprawa stanu klinicznego chorych z chorobą niedokrwienną serca [156]. Obserwacja ta potwierdza zasadność podawania odpowiednio wysokich dawek tego leku dla uzyskania istotnego wzrostu stężenia CoQ10 we krwi.
Dysponujemy ograniczoną liczbą badań kinetyki CoQ10 u ludzi (tab.1) [59, 89, 93, 94, 142, 177].
Po doustnym podaniu leku w dawce 100 mg stężenie maksymalne we krwi występuje po upływie 5-10 h (śr.6,5 h). Związane to jest prawdopodobnie z dużą masą cząsteczkową i słabą rozpuszczalnością tego związku w wodzie. Następnie związek dość szybko przemieszcza się z krwi do różnych tkanek i narządów.
Stwierdzono, że średnie stężenie egzogennego ubichinonu we krwi po jednorazowym doustnym podaniu 100 mg CoQ10 wynosiło 1.004 ± 0.37 mg/ml. Zawartość egzogennego CoQ10 we krwi po trzykrotnym spożyciu 100 mg leku w ciągu jednego dnia wzrosła do 5.4 mg/ml. Przekraczała więc średnie stężenie endogennego ubichinonu u ludzi zdrowych od 4 do 7 razy. Obserwacje Luckera i wsp.[177] wskazują, że ubichinon w zakresie zastosowanych dawek cechuje kinetyka liniowa.
Stężenie CoQ10 we krwi osób chorych, jak to wykazały liczne badania, jest często obniżone. Niektórzy autorzy polecają zatem jego rutynowe określanie w różnych stanach patologicznych. Kontush i wsp. [148] wykazali np., że pomiar stężenia koenzymu we krwi ( istotnie obniżony!) może być czułym markerem chorób wątroby.
Z organizmu wydala się głównie w formie macierzystej oraz częściowo zmetabolizowanej, przede wszystkim z kałem. Związek jest również w niewielkim stopniu eliminowany z moczem. Biologiczny okres półtrwania egzogennego CoQ10 wg tych autorów wynosi około 51 godz. Inni określili wartość tego parametru na 33.9 ± 5.32 h [93, 94]. Warto w tym miejscu podkreślić, że biologiczny okres półtrwania endogennego CoQ10 waha się w różnych narządach od 50 do 120 godz. [43].
Pola pod krzywą stężeń leku (AUC0-24h ), niezależnie od tego czy obliczano ich wielkość po podaniu jednorazowym, czy wielokrotnym, nie różnią się istotnie. Na tej podstawie założono, że przewlekłe podawanie CoQ10 nie stwarza możliwości jego nadmiernej kumulacji.
Podsumowanie
Egzogenny CoQ10 charakteryzuje się kinetyką podlegającą prawom modelu wielokompartmentowego. Najczęściej stosowany jest w formie preparatów doustnych o stosunkowo małej biodostępności. Dla uzyskania stężenia terapeutycznego we krwi wymagane jest więc stosowanie doustne odpowiednio wysokich dawek tego leku. Po wchłonięciu do krwiobiegu związek ulega dystrybucji do różnych tkanek i narządów, przy czym głównym miejscem magazynowania jest wątroba. Stopień gromadzenia się CoQ10 w innych narządach jest znacznie mniejszy. Biologiczny okres półtrwania egzogennego CoQ10 we krwi wynosi około 51 h. Lek wydala się z organizmu zarówno drogą przewodu pokarmowego, jak i z moczem, przede wszystkim w formie nie zmetabolizowanej.
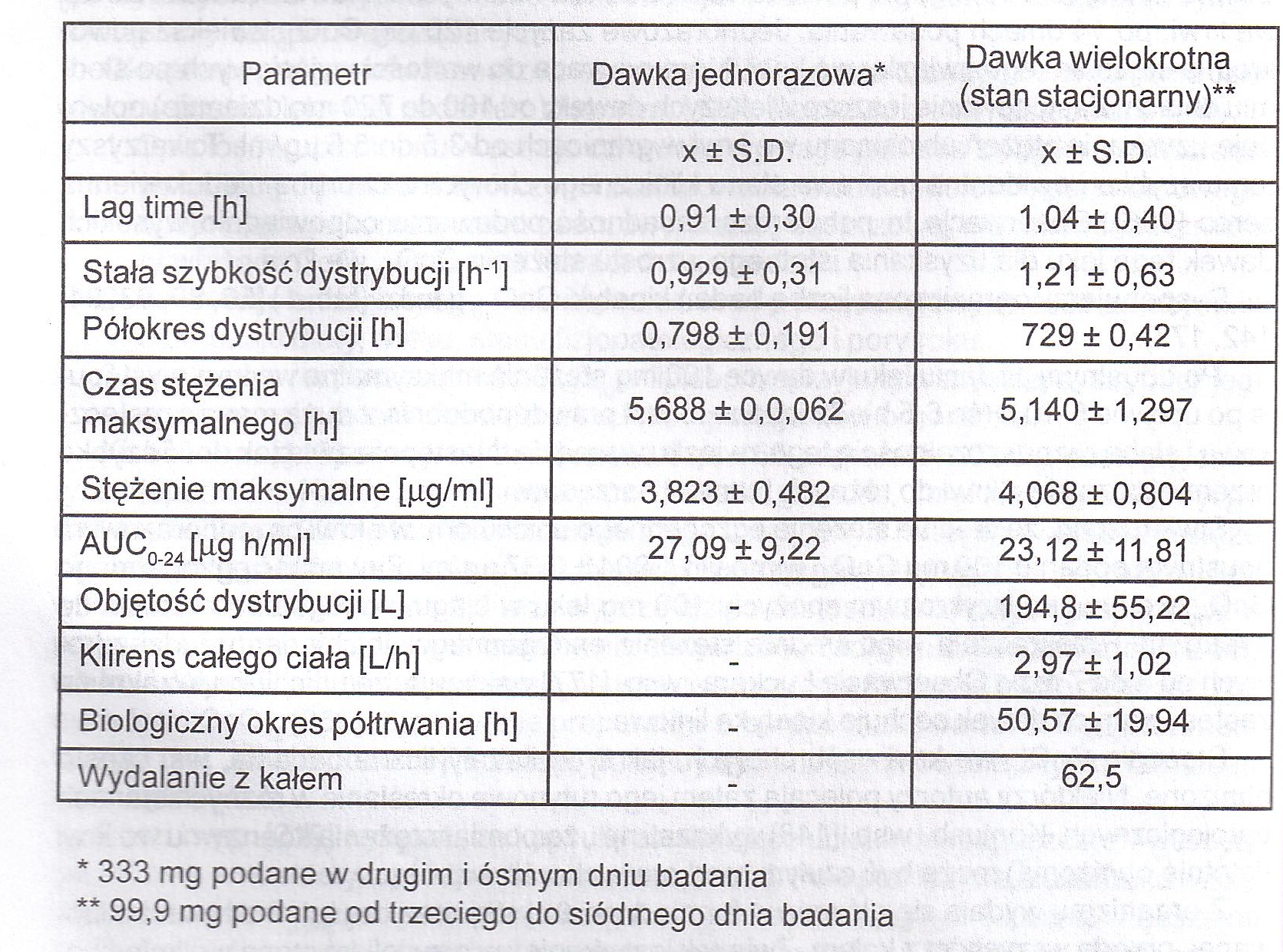
Tabela 1. Parametry farmakokinetyczne koenzymu Q10 wg Luckera i wsp.